比较常用的加速NAFLD和NASH动物模型的诱导方法,例如四氯化碳(CCl4)和蛋氨酸胆碱缺乏(MCD)饲料,以及第二代胆碱缺乏饲料。
开发临床前NASH纤维化模型
1. 使用四氯化碳进行炎症、脂肪变性和细胞死亡的毒素诱导
2. 通过MCD饲料诱导的肝脂肪变性
3. 增强NASH的新一代胆碱缺乏饲料,没有早期模型中观察到的重度体重减轻
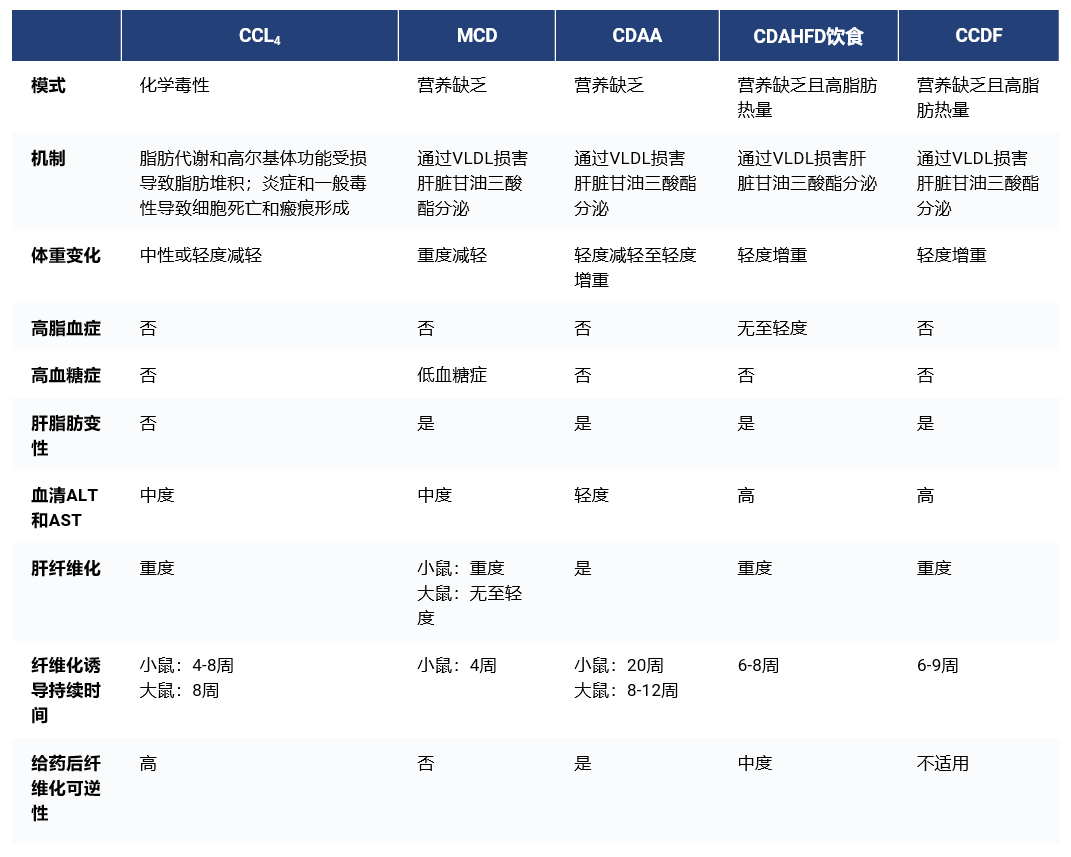
本文对比了这些传统纤维化模型,探讨它们在纤维化和NASH药物开发方面的优势和局限性。
四氯化碳诱导NASH模型
溶剂四氯化碳(CCl4)是一种毒素,通过肝脏细胞色素P450代谢为三氯甲基自由基(–CCl3)。这会与许多肝脏靶标发生反应,达到多种类似NASH的效应:
- 线粒体活性氧簇引发的炎症
- 脂代谢酶活性降低和高尔基氏体驱动的VLDL分泌受损导致的脂肪变性
- 广泛的细胞损伤,导致细胞死亡和纤维化
这些有害效应在没有肥胖或胰岛素抵抗的情况下发生,并且涉及大量与脂质贮积和代谢无关的细胞死亡。因此,这并不能代表真实的NAFLD。
除了缺乏对人类NAFLD/NASH的真正可译性外,该模型的主要缺点是影响非肝脏器官和组织的全身毒性,且由于CCI4对操作人员具有潜在化学危害,所以只能由训练有素的技术人员执行,必须配备适当的防护设备和化学安全基础设施。
MCD饲料诱导NASH模型
蛋氨酸和胆碱是肝线粒体β氧化和极低密度脂蛋白(VLDL)合成所需的关键营养素。喂食MCD饲料时,甘油三酸酯的输出受到抑制,从而迅速诱导肝脂肪变性和炎症。
和CCl4一样,MCD饲料因其易用性和快速诱导而广受欢迎。两周内血清ALT/AST稳健上升,并且临床NAFLD活性评分在同一时间段内接近最大值。纤维化也迅速发生,在短短4周内就很明显,10周内达到重度。在不超过16周的过程中,纤维化是可逆的,因此应在更长的时间范围内运行模型,以评价可改善NASH的药物。但是,动物选择比CCl4模型受到更多限制,C57Bl/6小鼠是首选的易感小鼠品系;大鼠会进展为稳健的脂肪变性,但只有轻微炎症,且没有纤维化。
MCD模型有许多转译和实践方面的缺点,最明显的是,动物经历了快速而严重的体重减轻(从喂食MCD饲料开始超过40%),以及血清葡萄糖、甘油三酸酯和胆固醇降低。体重减轻也造成操作人员在动物处置和给药方面的难度,而代谢表型则与人类状况直接相反。
第二代胆碱缺乏饲料诱导NASH模型
经证明,第二代胆碱缺乏饲料可在啮齿动物中诱导NAFLD/NASH,而不会出现MCD饲料饲喂时的重度体重减轻。胆碱缺乏性氨基酸(CDAA)饮食可以用精确等量的左旋氨基酸代替蛋白质含量,接受该饲料的C57Bl/6小鼠在3周内出现脂肪变性和炎症,纤维化发生在第6周,并在第21周左右变为轻度至中度,这也是可逆的。
这种饮食也适合Wistar大鼠诱导NAFLD/NASH,并且与小鼠的疾病发作和进展时间范围相近。尽管任何啮齿动物体重减轻都不是该模型的缺点,但是该模型中不存在NAFLD之前的人类代谢表型(胰岛素抵抗、高血糖症、脂血症等)。
CDAA饲料的热量脂肪含量从10-20%增加至60%(高脂胆碱缺乏饲料)会加速并加重NASH,并显著降低纤维化的自发可逆性。在C57Bl/6小鼠中,该模型还将在24周内发展为肝硬化、门静脉高压和肝功能衰竭,因此对于肝脏疾病研究项目而言具有多种用途。然而,在胆碱缺乏饮食的迭代中,没有肥胖、高血糖症和高甘油三酯血症等代谢综合征的特征。
结论
经典的CCl4肝脏毒性模型以及胆碱缺乏饲料诱导的脂肪变性的多次迭代,为NASH和肝纤维化提供了一套特征明确且广泛可用的啮齿动物模型。在选择四氯化碳或胆碱缺乏饮食模型时,应结合它们的优点,同时考虑其在人体条件下可译性方面的诸多局限性。
本文作者:中美冠科生物
 协同生物
协同生物






