慢性肾病(CKD)困扰着全球近8.5亿人,其一线治疗方法是饮食干预。已有研究证实,肠道菌群与慢性肾病进展相关,饮食中含硫氨基酸(Saa)的摄入量影响该疾病进展,但具体机制仍不明确。来自哈佛大学医学院的Wendy S. Garrett团队,利用小鼠慢性肾病模型研究了肠道微生物群和蛋白质摄入之间的机制联系,发现细菌对含硫氨基酸的代谢通过硫化物抑制色氨酸酶来调节吲哚的产生,从而消除该代谢物在该模型系统中的尿毒症毒性,并改善了小鼠慢性肾病的进展。研究结果于2020年9月发表在《Science》期刊上。
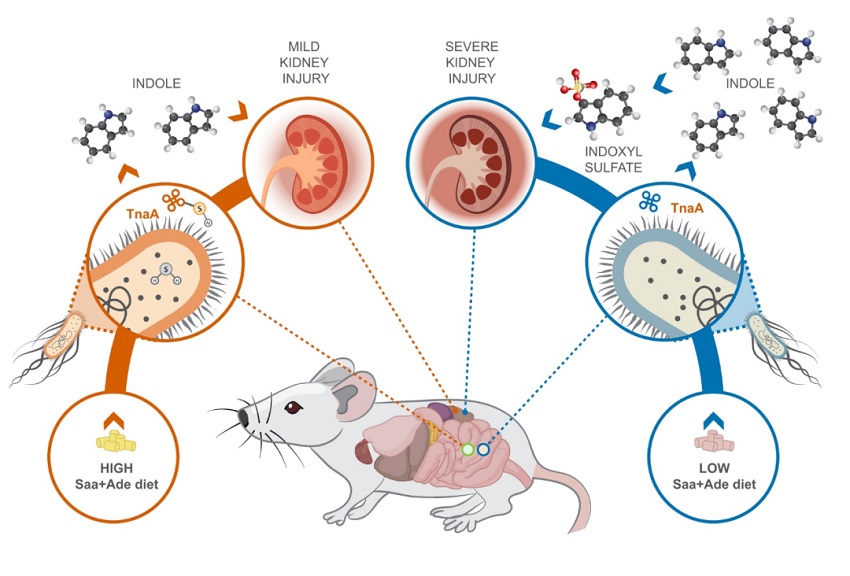
低含量Saa+Ade饮食和肠道菌群加剧慢性肾病进展
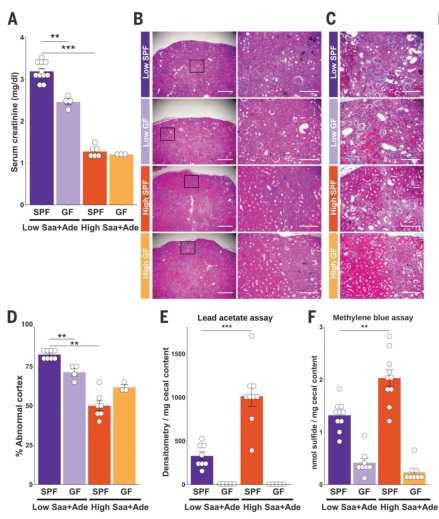
为验证含硫氨基酸的摄入可以改善慢性肾病,作者利用慢性肾病模型小鼠进行实验。通过高含量和低含量的硫氨基酸+腺嘌呤(Saa+Ade)饲料分别喂食SPF级小鼠、无菌小鼠,发现低含量Saa+Ade饲料组的SPF级小鼠的血清肌酐水平显著升高,出现严重肾皮质组织病理学变化,而同组的无菌小鼠的血清肌酐和肾损伤明显减少;高含量Saa+Ade饲料组的SPF级小鼠和无菌小鼠表型相似,证明低含量Saa+Ade饮食加剧了慢性肾病表型,肠道菌群进一步放大了这些影响。
用醋酸铅或亚甲蓝法检测SPF级和无菌小鼠盲肠硫化物水平,高含量Saa+Ade饲料组的SPF级小鼠盲肠硫化物水平高于低含量Saa+Ade饲料组,而无菌小鼠盲肠硫化物水平低于SPF级小鼠,说明肠道菌群将半胱氨酸代谢为H2S。使用16S核糖体RNA(rRNA)基因扩增子调查,低含量与高含量Saa饲料组的SPF级小鼠之间肠道菌群成员的分类丰度没有任何显著差异,说明健康小鼠盲肠硫化物的差异可能是由微生物功能的改变引起,而不是微生物群落结构的改变引起的。
大肠杆菌与饮食中的Saa相互作用减少肾损伤
人类慢性肾病患者样本的标准化大肠杆菌平均基因丰度高于非慢性肾病对照。在无菌小鼠中定植ASF菌群,或定植ASF菌群和大肠杆菌K-12,发现在低含量Saa+Ade饲料组,小鼠定植ASF和大肠杆菌(ASFE)具有更高的血清肌酐和更广泛的小管炎、小管萎缩和脱落、管周纤维化和皮质晶体,且盲肠硫化物水平较高。说明,大肠杆菌与饮食中的Saa相互作用调节肾功能。
TnaA可能是慢性肾病宿主与微生物相互作用的靶点
醋酸铅硫化物检测实验表明,需氧或厌氧生长的大肠杆菌以剂量依赖性方式从半胱氨酸中产生硫化物,而硫化物通过生成修饰半胱氨酸残基的多硫化物,导致S-硫化水合发挥作用。通过基于质谱的定量蛋白质组学分析,鉴定出212种s-硫酸化蛋白质,其中,色氨酸酶(TnaA)可以将色氨酸降解为吲哚、丙酮酸和氨,而已知吲哚参与细菌与宿主的相互作用,还可通过静脉转运至肝脏,在肝脏被氧化,产生尿毒症毒素硫酸吲哚酚,所以,TnaA成为研究慢性肾病小鼠模型中宿主-微生物相互作用的一个有吸引力的靶标。
Saa调节盲肠吲哚水平和肾功能
由于ASF细菌基因组均不编码TnaA基因,利用LC-MS/MS无法检测到ASF小鼠盲肠内容物中的吲哚,暗示了大肠杆菌是该模型中吲哚的唯一生产者,测定了两种饮食的ASF大肠杆菌小鼠盲肠内容物中的吲哚,发现接受高含量Saa饲料的小鼠吲哚水平显著降低,证明高含量Saa饮食不仅增加TnaAS-硫化,而且这种模式足以影响体内TnaA活性。
 协同生物
协同生物






